Пищевая аллергия лусс л в

Автор:
Лусс Л.В.
1
1 ФГБУ «ГНЦ Институт иммунологии» ФМБА России, Москва
Для цитирования: Лусс Л.В. Принципы терапии и профилактики пищевой аллергии. РМЖ. 2005;3:140.
Термин «Пищевая аллергия» (ПА), нередко используется медицинскими работниками (особенно в США) для обозначения побочных реакций на пищу различного генеза, в том числе, опосредованных иммунологически. Поэтому к пищевой аллергии относят очень разные по механизму развития состояния, такие как: истинная пищевая аллергия, анафилактический шок на пищевые продукты, ложная пищевая аллергия или псевдоаллергия, пищевая непереносимость, токсические реакции на пищу, фармакологические реакции на пищу. Клиницистам становится понятным, что такой подход к терминологии ПА, создает ряд проблем при определении тактики ведения больных с непереносимостью пищевых продуктов, столь разных по патогенезу.
С патофизиологических позиций к пищевой аллергии следует относить иммунологически опосредованные реакции непереносимости пищевых продуктов, обусловленных нарушениями в системе иммунитета. Они могут протекать как по гуморальным, так и клеточным механизмам аллергии, т.е. с участием аллергических АТ или сенсибилизированных лимфоцитов.
Актуальность ПА определяется не только чисто медицинскими проблемами, связанными с высокой распространенностью, тяжестью клинического течения, серъезностью прогноза, но и высокой социальной значимостью проблемы, требующей огромных финансовых затрат на лечение, реабилитацию, организацию социально–бытовых условий и питания пациентов.
По результатам стандартизированных эпидемиологических исследований, проведенных в разных странах мира, в том числе в России, 10% детского и 2% взрослого населения страдают ПА. Часто ПА наблюдается у больных с аллергическими заболеваниями. Так у 30–40% детей и 20% взрослых больных атопическим дерматитом выявляется ПА. При бронхиальной астме ПА выявляется в среднем у 17% больных.
Особенно часто ПА выявляется у больных с заболеваниями ЖКТ, печени и мочевыделительной системы, в среднем от 50 до 90%. Практически любой пищевой продукт может стать причиной развития ПА, но чаще она развивается при употреблении белков животного или растительного происхождения (табл. 1).
Основными источниками растительных пищевых аллергенов, имеющих важное значение в формировании ПА являются:
– PR (pathogen–response proteins) белки или «белки защиты»
– актин–связывающие (структуральные) белки или профилины
– тиоловые протеазы
– проламины: резервные белки семян и белки хранения (запаса).
PR (pathogen–response proteins) белки обладают, как правило, низкой молекулярной массой (ММ), стабильностью при низких значениях рН, устойчивостью к действию протеаз, обладают структурной общностью
Из 14 групп PR белков – 8 содержат аллергены, имеющие перекрестные реакции с различными пищевыми продуктами и важное практическое значение:
– PR2 белки – b–1,3,–глюконазы, защищают растения от грибковой инфекции. Выделенные из бразильской гевеи, они получили название Hev b 2. Эти белки имеют перекрестную чувствительность со многими овощами и фруктами (фруктово–латексный синдром).
– PR3 белки – эндохитиназы, гидролитически расщепляет хитин. Имеет перекрестную чувствительность с латексом, фруктами, овощами.
– PR4 белки – хитиназы, имеются в листьях табака, пораженных вирусом, аминокислотные последовательности (АК) последовательности гомологичны белкам сои, картофеля, томатов.
– PR5 белки – тауматин–подобные белки, защищают растения от засухи, грибковой инфекции. Первым выделен главный аллерген яблок, вишни, пыльцы горного кедра.
АК этого аллергена гомологичны с тауматином пшеницы, сладкого перца, томатов.
– PR8 белки, латексный минорный аллерген гевамин, идентичный лизоцим/хитиназе огурца.
– PR9 белки – лигнин–образующие пероксидазы. Выделен из пшеничной муки, с ним ассоциирована «астма булочников»
– PR10 белки, большая группа внутриклеточных белков из растений разных семейств (косточковые, пасленовые и др.). Структурная гомология с пыльцой березы, ольхи, орешника, каштана, граба, дуба и пищевых продуктов (каштана, фундука, желудя и др.).
– PR14 белки обеспечивают межмембранный перенос фосфолипидов из липосом к митохондриям. Обладают антибактериальной и противогрибковой активностью.
PR14 белки обладают выраженной перекрестной реактивностью. Первые PR14 белки были идентифицированы из пыльцы крапивы, к ним принадлежат аллергены из: персиков, абрикосов, слив, вишни, яблок,, винограда, лесного ореха, каштана.
Актин–связывающие (структуральные) белки или профилины.
Актин–связывающие (структуральные) белки регулируют сеть актиновых волокон, образующих цитоскелет растений. Эти белки впервые были идентифицированы из пыльцы березы и названы профилинами. Актин–связывающие белки обладают выраженными перекрестно–реагирующими свойствами со многими группами аллергенов и часто являются причиной анафилактических реакций, особенно у детей, на сою и арахис. С актин–связывающиими белками связывают развитие аллергических реакций на морковь, картофель, сельдерей, тыквенные семена, лесной орех, томаты и др. у больных поллинозом.
Тиоловые протеазы содержат папаин из папайи, фицин из винной ягоды, бромелайн из ананаса, актинидин из киви, соевый белок из сои, мышиные АТ к постельным клещам д.п. (клинической ассоциации с растительными тиоловыми протеазами не установлено)
Проламины: резервные белки семян и белки хранения (запаса). Многие резервные белки семян относятся к PR14 белкам. Белки хранения или собственно проламины – высокомолекулярные белки, растворимые в смеси вода/спирт.
Наличие перекрестных реакций между белками, содержащимися в различных пищевых продуктах, имеет особенно важное значение для больных с ИПА, поскольку у этих пациентов возможно развитие перекрестных аллергических реакций на другие группы аллергенов, например пыльцевые (табл. 2).
Перекрестные реакции также могут развиваться между пищевыми, бытовыми и эпидермальными аллергенами (табл. 3).
Особенности терапии и профилактики пищевой аллергии зависят от механизмов развития непереносимости пищевых продуктов, стадии и степени тяжести клинических проявлений, возраста больного, сопутствующих заболеваний и условий проживания пациента.
Общие направления терапии ПА включают: патогенетический подход, принцип комплексного лечения и этапность в проведении терапии.
Лечебно–профилактические мероприятия при ПА включают следующие основные положения:
Элиминационная диета при ИПА
• Рациональное питание при ЛПА
• Фармакотерапия (симптоматическая, базисная профилактическая терапия, лечение сопутствующих заболеваний)
• Аллерген–специфическая иммунотерапия
• Иммуномодулирующая терапия (при сочетании пищевой аллергии с иммунной недостаточностью)
• Образовательные программы (обучение медицинских работников, пациентов и их родственников в аллергошколе)
• Профилактика:
– Первичная
– Вторичная
– Третичная
Как известно, в случае истинной ПА ряд факторов может вызвать нарушение иммунного барьера кишечника, куда поступают огромные количества антигенов. Каковы эти акторы?
У новорожденных и младенцев: незрелость кишечника, – временный дефицит sIgA, атопический статус, факторы окружающей среды (курение родителей, загрязненность атмосферы, воды, почвы, продуктов питания и т.п.), – чрезмерное воздействие аллергенов (антигенов) на кишечник, – иммуносупрессорное воздействие вирусных инфекций.
У детей, подростков и взрослых к провоцирующим факторам ПА относятся: – любые заболевания и состояния, сопровождающиеся раздражением слизистой кишечника, паразиты, желудочно–кишечный кандидоз, алкоголь и др.
В связи с этим, большое внимание уделяется устранению (элиминации) причинно–значимых и провоцирующих факторов, способствующих развитию ПА.
Неиммунные компоненты барьера слизистых оболочек кишечника также играют значительную роль в формировании ПА, что следует учитывать при определении тактики ведения таких пациентов.. «Барьер слизистых оболочек ЖКТ» эффективно препятствует проникновению пищевых антигенов через кишечный тракт.
«Неиммунный барьер» представляют: кислотность желудочного сока, протеолитические ферменты и секрет поджелудочной железы, слизь кишечника.
Формированию ЛПА способствуют широкое использование в пищевой промышленности пищевых добавок, среди которых особое место занимают:
Пищевые красители: Тартразин (Е102), Желто–оранжевые (Е110), Эритрозин (Е–127), Азорубин (Е–122), Амарант (Е–123), Красная кошениль (Е–124), Бриллиантовая чернь BN (Е–151).
Консерванты: Бензойная кислота (Е–210), Бензоаты (Е 211–219), Сульфиты и их производные (Е 220–227), Нитриты (Е 249–252).
Вкусовые добавки: Глутамат натрия (Е–621), Глутамат калия (Е–622), Глутамат кальция (Е–623), Глутамат аммония (Е–624), Глутамат магния (Е–625).
Ароматизаторы: Глутаматы (В 550–553).
Пока нет убедительных данных о безопасности генетически модифицированных продуктов, их нельзя употреблять больным с ПА.. Генетически обработанная (манипуляционная) или (GM) пища – качественно новые продукты, полученные путем генетической обработки (соевые бобы, картофель, кукуруза и др.) с использованием современных новых технологий.
Ниже перечислены продукты, в состав которых часто входит тартразин. Эти продукты следует ограничивать или полностью исключать (если есть аллергия) из питания больных ПА.
• Хлопья
• Макаронные изделия, не содержащие яиц
• Готовые смеси для приготовления теста
• Готовые пироги, пряники, коврижки, глазурь, пудинги
• Замороженные хлебобулочные изделия, хлеб из теста быстрого приготовления
• Шоколадная стружка
• Жареный хрустящий картофель, окрашенный в оранжевый цвет
• Окрашенные газированные и фруктовые напитки
• Цветной зефир
• Карамель, драже
• Обертка для конфет
Продукты, содержащие сульфиты, также следует ограничивать больным с ИПА и ЛПА. Их перечень представлен ниже.
• Салаты из помидоров, моркови, перца, латука
• Свежие и сухие фрукты (в частности, косточковые)
• Вина, пиво, наливки, ликеры
• Безалкогольные шипучие напитки (алкогольные – тоже), произведенные из виноградного сока
• Фруктовые соки
• Желатин
• Глюкоза кристаллическая и в виде сиропа
• Смеси для выпечки
• Маринады и соления, уксус
• Сушеные овощи
• Консервированные овощи, супы, сухие суповые смеси, морепродукты
• Соусы: к мясу, рыбе, из авокадо и др.
• Сыры
• Свежая рыба
• Колбасный фарш
При ИПА больным следует назначать элиминационные диеты с полным исключением причиннозначимых пищевых аллергенов и других продуктов, в состав которых они могут входить. При назначении элиминационных диет важно не только указать какие продукты исключаются из питания, но и предложить пациенту перечень пищевых продуктов, которые можно включать в диету. Элиминационная диета по объему и соотношению пищевых ингедиентов должна полностью соответствовать возрасту больного, сопутствующим заболеваниям и энергетическим затратам.
Варианты диет при пищевой аллергии
1. Беззлаковая диета (исключить крупы, муку и мучные изделия, приправы, соусы и др.).
Можно: мясо, рыба, овощи, фрукты, яйца, молочные продукты и др. (при отсутствии аллергии к ним).
2. Диета с исключением яиц (исключить яйца и приправы, майонез, кремы, соусы, кондитерские, макаронные и хлебобулочные изделия с содержанием яиц)
Можно: мясо, молочные продукты, крупы, муку и мучные изделия без яиц, овощи, фрукты (при отсутствии аллергии к ним).
3. Диета с исключением молока (исключить молоко и мол. продукты, каши на молоке, сгущенку, творог, сметану, кондитерские, макаронные и хлебобулочные изделия с содержанием молока), слив.масло, сыры, конфеты, содержащие молоко.
Можно: мясо, рыба, яйца, крупы, овощи и фрукты, мучные изделия без молока и др. (при отсутствии аллергии к ним).
4. Диета с исключением молока, яиц и злаков (исключить продукты, содержащие молоко, яйца, пищевые злаки).
В настоящее время имеется большой выбор продуктов питания для больных ИПА и ЛПА, как для детей, так и взрослых. В частности, уже более полувека западногерманская фирма HUMANA предлагает программу детского питания, включающую лечебные и профилактические продукты и продукты прикорма. Большинство продуктов, входящих в него, может применяться для детей различного возраста и взрослых. В разработке состава смесей учитываются все новейшие достижения и требования ВОЗ и Европейского общества педиатров, гастроэнтерологов и диетологов (ESPGAN). Для младенцев с повышенным риском к аллергии, а также для детей с пищевой аллергией, непереносимостью белков сои, начиная с первых дней жизни можно рекомендовать – Humana HA1. Применение – Humana HA1: как единственное питание, у детей на искуственном вскармливании, как дополнение к кормлению грудью, сразу же после кормления грудью или любого другого гипоаллергенного молочного питания для младенцев .
Humana HA2 рекомендована детям после 4 месяцев с повышенным риском аллергии и содержит расщепленные белки, хорошо насыщает и усваивается, без белого сахара–песка, не содержит глютена и обогащена пребиотиками – галактоолигосахаридами, которые являются энергетическим сустратом для нормальной флоры кишечника. Применение – Humana HA2: если младенец не насыщается больше Humana HA1, сразу же после кормления грудью или любого другого гипоаллергенного питания для младенцев, в рамках смешанного питания.
Humana HA Каша – специальная гипоаллергенная каша для детей после 4–го месяцев и взрослых. Применение Humana HA Каша: как дополнение к кормлению грудью, к Humana HA1, Humana HA2 или любому другому питанию для младенцев, как лечебное питание.
При аллергии к коровьему молоку рекомендовано использование специального питания – Humana SL. Оно изготовлено на основе растительного белка, его можно давать начиная с первой бутылочки вплоть до школьного возраста. Humana SL не содержит коровьего молока, молочного белка, галактозы, белого сахара–песка, клейковины.
При непереносимости сывороточных белков и сопутствующей патологии ЖКТ можно рекомендовать программу –Humana HN лечебное питание.
Расчет Humana HN лечебное питание на одно кормление зависят от индивидуальных особенностей ребенка и взрослых (табл. 4).
Существуют и другие программы питания для детей и взрослых, выпускаемые отечественными и зарубежными фирмами, которые назначаются с учетом показаний и противопоказаний к их применению.
Больным с ЛПА, особенно в период обострения, назначается гипоаллергенная диета с исключением продуктов, богатых гистамином, тирамином, гистаминолибераторами. К ним относятся: рыба, рыбные продукты, морепродукты (крабы, креветки и тп), яйца, ферментированные сыры, вина, пиво, острые блюда, копченности, прянности, продукты с высоким содержанием тартразина, сульфитов (см. выше) и др.
При назначении гипоаллергенной диеты больным ЛПА необходимо точно указать длительность ее применения и порядок расширения диеты после устранения симптомов непереносимости пищевых продуктов.
Фармакотерапия при пищевой аллергии назначается в острый период для устранения симптомов развившейся реакции и базисная терапия для профилактики развития таких реакций. В острый период назначаются антигистаминные препараты, дозы и способ введения которых (внутрь или парантерально) определяются степенью тяжести реакции. В тяжелых случаяах (системные реакции, отек Квинке жизнеугожающей локалазации и тп) назначаются глюкокортикостероиды в возрастной дозировке.
Антигистаминные препараты: 1. Препараты блокирующие гистаминовые рецепторы (Н1–рецепторы).
2. Препараты, повышающие способность сыворотки крови связывать гистамин (гистаглобин, гистаглобулин и др.), назначают с профилактической целью . В настоящее время они применяются реже, так как для неспецифической терапии имеются медикаменты с меньшими побочными эффектами, не содержащих белка.
3. Препараты, тормозящие высвобождение гистамина из тучных клеток: кетотефен, кромолин–натрий и др. Эта группа препаратов назначается с профилактической целью на длительный срок, не менее 2–4 месяцев.
Как при ИПА, так и при ЛПА необходимо своевременно проводить коррекцию сопутствующих заболеваний ЖКТ, гепатобилиарной системы и др. (ферменты, пробиотики, энетросорбенты и тп).
Отношение к проведению АСИТ у больных ИПА пока не однозначно и противоречиво. В основном, предпочтение отдается назначению элиминационных диет.
Профилактика ПА направлена на устранение, насколько возможно – полное, причинозначимых аллергенов, факторов риска и провоцирующих факторов с учетом возраста, наличия генетически детерминированной предрасположенности к развитию аллергии и сопутствующих соматических заболеваний.
Прежде чем назначить терапию по поводу ПА, следует исключить другие заболевания, которые по клиническим симптомам напоминают аллергические реакции на пищу, такие как: желудочно–кишечные заболевания, психические нарушения, метаболические нарушения, интоксикации, инфекционные заболевания, аномалии развития желудочно–кишечного тракта, недостаточность экзокринной функции поджелудочной железы, целиакия, ИДС, передозировка лекарственных средств, дисахаридазная недостаточность, эндокринная патология, синдром раздраженной кишки.
Поделитесь статьей в социальных сетях
Источник

Пищевая аллергия – это одно из наиболее распространенных аллергических состояний, обусловленное непереносимостью соединений в составе некоторых продуктов питания. Проявления заболевания разнообразны: кожные симптомы (высыпания, зуд, крапивница), нарушения функции ЖКТ (диспепсические расстройства), иногда возможны системные анафилактические реакции. Диагностика производится посредством постановки кожных аллергологических проб, изучения анамнеза и пищевого дневника больного, выполнения лабораторных анализов. Лечение заключается в элиминации провоцирующих продуктов из рациона пациента, назначении антигистаминных средств, в редких случаях – десенсибилизирующей иммунотерапии.
Общие сведения
Пищевая аллергия является самой частой аллергопатологией, что обусловлено значительным разнообразием веществ, входящих в состав продуктов питания человека. Примерно половина больных – дети в возрасте до 12 лет, у старших лиц распространенность заболевания снижается. Более частое возникновение болезни у детей объясняется контактами с новыми для организма антигенами и повышенной реактивностью в данный период жизни. В дальнейшем на большинство соединений пищи вырабатывается иммунологическая толерантность, и проявления аллергии встречаются намного реже. Существует генетическая предрасположенность к развитию данного состояния, имеющая полигенный характер. В отдельных случаях непереносимость определенных продуктов сохраняется всю жизнь и может осложняться перекрестными реакциями и иными аллергическими состояниями (к примеру, бронхиальной астмой).
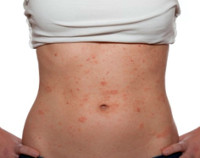
Пищевая аллергия
Причины
Большая часть случаев заболевания обусловлена гиперчувствительностью первого типа, опосредованной выделением IgE и активацией тканевых базофилов. Непосредственной причиной патологии является попадание в желудочно-кишечный тракт белковых соединений, которые распознаются иммунитетом и запускают его аномальный ответ. Выявлено огромное количество предрасполагающих к пищевой аллергии состояний и особенностей организма, часть которых характерна только для детей. Это является еще одной причиной частого развития аллергической реакции в детской популяции. Среди наиболее распространенных факторов, способствующих возникновению пищевой непереносимости, выделяют:
- Особенности аллергена. Гиперреактивность чаще вызывают антигены пищи, обладающие высокой иммуногенностью и способные без деградации преодолевать барьеры пищеварительной системы (в частности, агрессивную среду желудка). Большая часть из них содержится в коровьем молоке, рыбе, белке яиц, злаках, некоторых фруктах (клубника, цитрусовые) и орехах. Порядка 80% всех случаев заболевания обусловлено гиперчувствительностью к данным продуктам.
- Генетические факторы. Развитие непереносимости может быть обусловлено наследственными и генетическими свойствами организма. Они могут проявляться повышенным уровнем реактивности, аномальной активностью иммунитета и другими состояниями, облегчающими развитие аллергических реакций.
- Возрастные особенности ЖКТ. Возникновению аллергии на продукты способствуют наблюдаемая у детей высокая проницаемость стенок желудочно-кишечного тракта, низкая кислотность желудочного сока, нарушения состава микрофлоры кишечника. Эти условия облегчают контакт аллергена с иммунокомпетентными клетками, запускающими аллергический процесс.
На вероятность возникновения заболевания также влияет количество попавшего внутрь организма аллергена, характер кулинарной обработки продуктов, содержащих в себе провоцирующие вещества. Непереносимость продуктов может быть следствием перекрестной аллергии на пыльцу растений или бытовую пыль. Сенсибилизацию организма при этом вызывают антигены, переносимые по воздуху, но реакцию могут инициировать и продукты питания, имеющие схожие соединения в своем составе.
Патогенез
В процессе развития пищевой аллергии первоначально возникает сенсибилизация организма – она происходит при первом контакте с аллергеном. Последний распознается клетками иммунитета, которые через ряд промежуточных реакций вызывают образование иммуноглобулинов класса Е, специфичных к данному белковому соединению. Антитела такого типа обладают свойством адсорбироваться на поверхности тканевых базофилов, оставаясь там длительное время. При повторном поступлении провоцирующего антигена он связывается с IgE, которые активируют тучные клетки, вызывая их дегрануляцию с выходом гистамина. Этот биогенный амин обуславливает расширение кровеносных сосудов, отек тканей, раздражение нервных окончаний – данные изменения проявляются кожным зудом, крапивницей, диспепсическими расстройствами.
Особенностью аллергии к пищевым компонентам в младенческом возрасте является исключение этапа сенсибилизации из патогенетической цепи заболевания. Антитела против аллергена попадают в организм ребенка трансплацентарно или с грудным молоком от матери, которая страдает от непереносимости некоторых продуктов. По этой причине женщинам с аллергией особенно важно контролировать свое питание в период беременности и кормления грудью – в противном случае существует риск развития патологии у младенца. Но длительность такого состояния у детей незначительна – материнские антитела полностью элиминируются из организма через несколько недель после прекращения естественного вскармливания.
Симптомы пищевой аллергии
Клиническая картина патологии довольно разнообразна, статистически чаще регистрируются кожные симптомы, возникающие в течение 2-х часов после приема пищи. Развивается зуд, высыпания различной локализации, обычно эритематозного характера. Часть пациентов жалуется на крапивницу и иные отечные явления на поверхности кожи. В зависимости от тяжести аллергии и характера провоцирующего вещества эти симптомы могут сохраняться на протяжении нескольких часов или дней. После этого, при условии отсутствия контактов с аллергеном, кожные проявления обычно полностью и бесследно исчезают. При продолжении употребления опасного продукта аллергическая реакция регистрируется вновь, причем каждый новый эпизод характеризуется все более выраженными и тяжелыми симптомами.
Пищевая аллергия может проявляться нарушениями ЖКТ в первые часы после употребления аллергенных продуктов. Больные жалуются на боли в животе, тошноту, иногда рвоту и диарею. При особенно высокой аллергической готовности организма данные симптомы способны развиваться уже в момент приема пищи. Диспепсия сопровождается отеком слизистых оболочек полости рта, губ, поверхности языка. Иногда такой аллергический процесс приводит к заложенности носа, слезотечению, конъюнктивиту, что создает ложную картину поллиноза или непереносимости бытовой пыли.
Отдельные продукты питания (арахис, некоторые виды рыб, клубника) содержат аллергены, вызывающие сильные системные реакции – ангионевротический отек и анафилактический шок, сопровождающиеся спазмом гортани и падением артериального давления. У больных бронхиальной астмой гиперчувствительность к компонентам пищи может спровоцировать развитие приступа по механизму перекрестной аллергии. Ряд больных отмечает появление головных болей, повышенной утомляемости и слабости после употребления блюд с провоцирующими продуктами.
Осложнения
Наиболее тяжелым осложнением пищевой аллергии является анафилактический шок, вызванный массированной дегрануляцией базофилов и выделением большого количества гистамина. Он возникает при предрасположенности к непереносимости определенных продуктов или при длительном игнорировании проявлений заболевания. Продолжающееся поступление аллергена в организм приводит к постепенному нарастанию симптомов и в конечном итоге провоцирует развитие шока. Если аллергия сопровождается рвотой или диареей, то длительный контакт с антигеном может приводить к электролитным нарушениям. Среди других осложнений можно выделить возникновение перекрестной непереносимости антигенов цветочной пыльцы или бытовой пыли, инфицирование кожи в результате расчесов и повреждений.
Диагностика
Определение пищевой аллергии производится аллергологом-иммунологом, при этом важен тесный и доверительный контакт врача с пациентом или его родителями (при развитии патологии у детей). Для диагностики заболевания используют данные анамнеза, результаты лабораторных и иммунологических исследований, а также провокационных тестов. Последние следует использовать только в случае относительно низкой реактивности организма и легкости проявлений аллергии. При наличии риска системных реакций (отека Квинке или анафилактического шока) проведение исследований, предусматривающих контакт пациента с аллергеном, запрещено. Подтверждение диагноза и определение провоцирующего продукта проводят по следующему алгоритму:
- Осмотр и сбор анамнеза. Осматриваются кожные покровы больного для определения характера и выраженности высыпаний, в спорных случаях может потребоваться консультация дерматолога. Анализируется пищевой анамнез: выясняется, какие продукты употреблялись в последние дни и в каком количестве. На основе этого ограничивается круг возможных аллергенов, что облегчает дальнейшие исследования.
- Лабораторные анализы. В общем анализе крови незначительная эозинофилия определяется лишь при сильных либо неоднократных эпизодах аллергии. По показаниям микроскопическому исследованию подвергают смывы носоглотки, мазки-отпечатки с конъюнктивы – в них также обнаруживаются эозинофилы. Биохимическое исследование крови выявляет высокий уровень иммуноглобулинов классов E и G.
- Кожные аллергологические пробы. Для точного определения аллергена используют аппликационные пробы или прик-тест. При этом на кожные покровы наносят эталоны антигенов, попавших под подозрение в ходе расспроса больного. Развитие покраснения и отека является положительной реакцией и указывает на наличие непереносимости аллергена.
- Иммунологические анализы. К ним относят твердофазный иммуноферментный тест (ELISA) и радиоаллергосорбентный тест (RAST). Их проводят для определения типа провоцирующего антигена при высокой реактивности организма, когда кожные пробы исключены. Эти анализы с высокой точностью определяют наличие специфических к аллергену IgE в крови больного
Дифференциальную диагностику пищевой аллергии следует проводить с иными заболеваниями аллергического характера (поллиноз, атопический дерматит) и кожными патологиями (экзема, инфекционные поражения). При развитии диспепсических расстройств необходимо исключить риск пищевой токсикоинфекции или других болезней пищеварительной системы. Иногда симптомы, схожие с проявлениями аллергии, могут возникать из-за употребления непривычных или экзотических блюд. Обычно данные состояния самопроизвольно исчезают за несколько часов и редко возникают повторно.
Лечение пищевой аллергии
Лечебные мероприятия в практической аллергологии включают три этапа: облегчение симптомов аллергии, ускорение элиминации аллергена и предотвращение последующих контактов с ним. При непереносимости незаменимых продуктов питания используется десенсибилизирующая иммунотерапия. Важно также учитывать риск перекрестных реакций, поэтому после выявления аллергена специалист может ограничить потребление сразу ряда блюд. Их исключение из рациона надежно гарантирует отсутствие новых эпизодов пищевой аллергии. Основные этапы лечения складываются из:
- Симптоматической терапии. Применяют антигистаминные средства в различных формах выпуска – в виде таблеток, сиропов (в педиатрической практике) и назальных спреев. В большинстве случаев однократного приема препаратов данной группы достаточно для полного устранения проявлений пищевой аллергии. При более тяжелом течении специалистом может быть назначено их курсовое применение.
- Элиминации аллергена из организма. Может обеспечиваться как назначением специальной гипоаллергенной диеты, так и фармакологическими методами. В случае недавнего (несколько часов) попадания провоцирующего продукта в ЖКТ эффективны энтеросорбенты – активированный уголь, полисорб. Они связывают антигены в просвете кишечника, не позволяя им проникать в системный кровоток. Если после проникновения аллергенов прошло несколько дней, или они поступали в организм на протяжении длительного времени, то их элиминация возможна только естественным путем. Несколько ускорить ее можно инфузионной терапией или назначением диуретиков.
- Аллерген-специфической иммунотерапии (АСИТ). Этот этап лечения возможен только после полноценной диагностики патологии и точного определения провоцирующего антигена. Назначается в случае, если перечень запрещенных продуктов слишком обширен, или в него попадают незаменимые компоненты пищи. АСИТ заключается во введении постепенно повышающихся дозировок аллергена с целью выработки иммунологической толерантности к нему.
Прогноз и профилактика
Прогноз пищевой аллергии благоприятный, особенно при развитии состояния в детском возрасте – по мере роста ребенка непереносимость продуктов постепенно исчезает и практически не проявляется в дальнейшем. В случае наличия тяжелых реакций на арахис, морепродукты и некоторые фрукты довольно часто пациентам приходится пожизненно отказываться от их употребления. Кроме того, им рекомендуется иметь при себе средства для первой помощи при анафилактическом шоке (например, специальный шприц-ручку с адреналином). Профилактика сводится к ограничению использования продуктов высокого аллергического риска в детском питании и при беременности, а при наличии реакций – к их полному изъятию из рациона.
Источник
